| |
|
|
UVOD
Atrijalna fibrilacija (AF) je najčešća hronična aritmija [1] .
Učestalost javljanja atrijalne fibrilacije povećava se sa starošću,
ima prevalencu 5–10% kod osoba preko 60 godina i više od 15% kod
osoba preko 80 godina. AF se prezentuje različitim simptomima a oko
30% pacijenata su asimptomatski [2].
Kliničke manifestacije atrijalne fibrilacije kreću se od potpuno
asimptomatske aritmije otkrivene slučajno pri rutinskom odlasku kod
lekara, preko aritmije sa minimalnim, problematičnim,
onesposobljavajućim ili katastrofalnim simptomima, do hronične
aritmije koja takođe može davati minimalne ili onesposobljavajuće
simptome, što klasifikuje težinu simptoma AF prema EHRA skoru [2].
AF je udružena sa petostrukim povećanjem rizika od trombo-emboljskog
možanog udara a 1,5 put je veći rizik od fatalnog možadnog udara [3,
4, 5].
Atrijalna fibrilacija (AF), prema nivou rizika za tromboembolizam
zahteva uvođenje dugotrajne oralne antikoagulantne terapije (OAKT)
najčešće dikumarolskim preparatima, to jest antagonistima vitamina K
(VKA). Predstavnici ove grupe lekova su acenokumarol, varfarin, i
retko fenprokumon [6, 7]. Odluka o uvođenju OAKT donosi se na osnovu
opšte prihvaćenog CH2DS2VASc skora [2, 8]. Prikazana je u tabeli 1.
Tabela 1. CHA2DS2-VASc skor: Klinički
faktori rizika za moždani udar, tranzitorni ishemički atak i
sistemski embolizam
Tabela 1. CHA2DS2-VASc scor: Clinical risk factors for
stroke, transient ischaemic attack and systemic embolism

Oralna antikoagulantna terapija (OAKT, OAC) signifikantno
redukuje rizik od moždanog udara za više od 68% [9].
Mada antikoagulantna terapija povećava rizik od krvarenja, ona
obezbeđuje opšti benefit za pacijenta i pokazala se efikasna u
smislu cene i efektvnosti [2, 3, 9]. OAKT je preporučena Vodičima za
pacijente sa umernim i visokim rizikom za moždani udar koji nemaju
kontraindikacije (Tabela 2). Takođe, korišćenje direktnih,
pravilnije ne-vitamin K oralnih antikoagulansa (NOAK, NOAC) sve više
se uvećava, ali bez velikih studija praćenja dugotrajnog lečenja
[10, 11].
Antitrombocitni lekovi su ranije bili preporučeni za pacijente sa
niskim rizikom za moždani udar (CH2DS2-VASc skor =1), ali postoje
neki dokazi o neefikasnosti aspirina. Efektivni tretman sa VKA
zahteva monitoring protrombinskog vremena (PT) i izračunavanje
internacionalnog normalizovanog odnosa (INR) i prema njemu stalno
podešavanje terapijske šeme. Internacionalne serije bolesnika
ukazuju na veliki broja pacijenata (više od 50%) bez uvedene
antikoagulante terapije [2, 6, 7, 12]. Kontrola frekvence i ritma je
paralelni važan aspekt u lečenju atrijalne fibrilacije. [2, 5].
Paroksizmalna, perzistentna i permanentna forma aritmije zahtevaju
različiti terapijski pristup. Patofiziološki gledano, procesi
električnog i anatomskog remodelovanja miokarda prvenstveno leve
pretkomore dovode do skolnosti za nastanak tromba, prvenstveno
aurikule leve pretkomore i do oštećenja mehaničke funkcije
pretkomora i komora. Podrazumeva se zaključak da terapija mora biti
prilagođena svakom pacijentu pojedinačno u zavisnosti od sledećih
faktora: da li pacijent ima simptome, koliko su ozbiljni simptomi i
kolika je mogućnost vraćanja u sinusni ritam. Glavni ciljevi
terapije su: prevencija tromboembolizma, kontrola komorskog
odgovora, vraćanje u sinusni ritam i njegovo održavanje, kao i
prevencija recidiva AF [1, 2]. Merenje protrombinskog vremena krvi
(PT) i određivanje internacionalnog normalizovanog odnosa (INR)
aktuelnog PT prema svedoku daje meru optimalnog antikoagulantnog
efekta kada je INR od 2,0 do 3,0.
HAS-BLED skor [13] (Tabela 2) je razvijen zbog procene rizika od
krvarenja 2010 godine na 3978 pacijenata, koji vrši stratifikaciju
rizika na nizak skor 0-2 boda i visok rizik 3-9 za krvarenje. On
nalaže oprez sa OAKT uz smanjenje rizika od krvarenja redovnom
kontrolom INR, lečenjem hipertenzije, isključivanje komedikacije i
alkohola, zaštita blokatorima protonske pumpe, ali ne isključuje
uvođenje antikoagulantne terapije, osim u slučaju kontraindikacija
(Tabela 3).
Tabela 2. HAS-BLED skor za procenu
jednogodišnjeg rizika major krvarenja kod bolesnika sa AF na
antikoagulantnoj terapiji
Table 2. HAS-BLED scor estimates one year risk of major
bleddding for patients with atrial fibrillation on anticoagulation
therapy

U novom ESC vodiču za AF [2] proširen je broj rizik faktora za
krvarenje u antikoagulisanih pacijenata sa AF i podeljeni su na
promenjive (koji mogu da se modifikuju - hipertenzija, labilni INR,
lekovi, ekces alkohola) na potencijalno promenjive (anemija,
oštećenje funkcije jetre i bubrega, trombocitopenija ili oštećenja
funkcija trombocita) i nepromenjive (starost, predhodno veliko
krvarenje i predhodni moždani udar, bolesnici na hemodijalizi ili sa
transplantiranim bubregom, ciroza jetre, maligniteti i genetski
faktori). Dodati su i biomarkeri za rizik od krvarenja: Hs-Troponin,
Faktor diferenciranja rasta-15 (Growth differentiation factor-15) i
procenjena brzina glomerulske filtracije-eGFR ili klirens
kreatinina- CrCl.
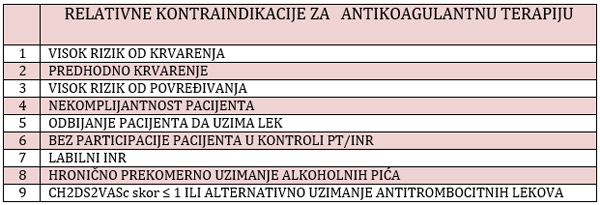
Tabela 3. Relativne kontraindikacije za
antikoagulantnu terapiju
Table 3. Relative contraindication for anticoagulation
therapy
MATERIJAL I METODE RADA
Ovom longitudinalnom, prospektivnom studijom je obuhvaćeno
konsektivnih 87 bolesnika sa atrijalnom fibrilacijom na OAKT. Na
acenokumarolu je bilo 68/87 (78%) bolesnika a na varfarinu 19/87
(22%). Predhodno su isključeni bolesnici koji su bili na
ne-dikumarolskim, novim antikoagulantnim lekovima (NOAK, NOAC).
Vreme u terapijskom opsegu (TTR) nije moglo da se izračuna kod
većine ispitanika metodom Rosendaal [14], niti alternativnom metodom
iz ROCKET AF studije [15] zbog malog broja merenja u toku godinu
dana oko 7 zbog nesaradnje pacijenata . Zato je razvijena i
korišćena orginalna klinička metoda-aproksimacija, na osnovu
kliničkih kriterijuma vrednosti INR. Kriterijumi za odličnu
antikoagulisanost je bio da u toku godinu dana većina vrednosti tj.
5 do 7 izmerenih vrednosti PT/INR bude ≥ 2 (analogno TTR >60-85%
vremena). Dobra anti-koagulisanost je definisana da 3 do 4 vrednosti
PT INR tokom praćenja od godinu dana budu u terapijskom opsegu
(analogno TTR 50 do 60% vremena). Slaba antikoagulisanost je
definisna da 0-2 izmerene vrednosti INR budu u terapijskom opsegu
(analogno TTR<50 %).
Svim bolesnicima su u toku godinu dana praćenja uz rutinske kliničke
i laboratorijske parametre, određivani indeks telesne mase (BMI),
obim struka, merenje krvnog pritiska, EKG i ehokardiografija.
Ehokardiografsko ispitivanje je vršeno na aparatu Toshiba Xario CV i
GE-Vivid 7 dimension. Sistolna funkcija je predstavljena ejekcionom
frakcijom leve komore. Ejekciona frakcija je normalna ukoliko je
veća od 50%, granična (mid range) od 40-49% i snižena ukoliko je
manja od 40 %. Dijastolna funkcija je najbolje reprezentovana
odnosom transmitralne E brzine i srednje brzine e’ mitralnog anulusa
na tkivnom Doppleru-E/e’. Taj odnos E/e’može da bude normalan,
graničan i povišen. Takođe je praćena i masa leve komore i dijametar
leve pretkomore. Masa leve komore je automatski dobijana
kombinovanim merenjem M-mod/Bmod formulom po Teicholzu uz
indeksiranje na telesnu površinu (indeks mase miokarda leve
komore-LVMI). Referentne vrednosti za hipertrofiju leve komore jesu:
LVMI >95 g/m2 za ženski pol a LVMI>115 g/m2 za muški pol. Dijametar
leve pretkomore je dobijen kombinovanim direktnim merenjem M-mod/B
mod sa normalnim vrednostima: <38 mm za ženski pol i <40 mm za muški
pol. Volumen indeks leve pretkomore (LAVI) nije svima rađen i ti
podaci nisu prikazani.
REZULTATI
U toku praćenja od godinu dana, na osnovu sukcesivnih vrednosti
PT/INR, 87 bolesnika sa atrijalnom fibrilacijom (AF) je
klasifikovano u tri grupe: grupa A - odlična kontrola - kvalitet
antikoagulantnog efekta N=14/87 (16%), grupa B - dobra kontrola -
kvalitet antikoagulacije N=24/87 (28%), grupa C - slaba kontrola -
kvalitet antikoagulantnog efekta N=49/87 (56%) što je prikazano u
Tabeli 4 i grafikonu 1.
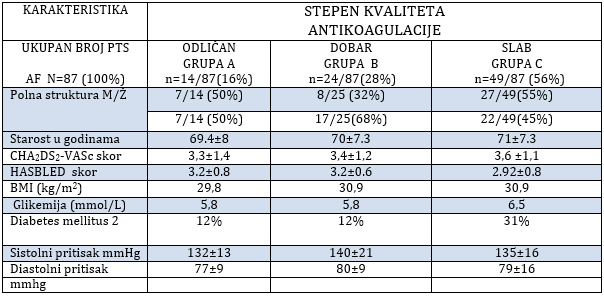
Tabela 4. Osnovne kliničke i laboratorijske
karakteristike kod 87 pacijenata podeljenih u 3 grupe prema
kvalitetu antikoagulantne terapije
Table 4. Baseline clinical and laboratory characteristics of
87 patients divided in 3 groups according to quolity of
anticoagulation therapy
Prevalenca cerebrovaskularnih inzulta na početku praćenja bila je
7/102 (6,9 %). Prevalenca velikih-major krvarenja bila je 2/102 (1,9
%) u oba slučaja gastrintestinalana (melena).
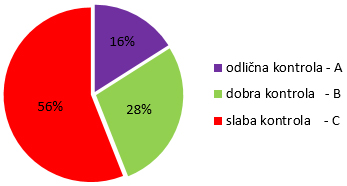
Grafikon 1. Antikoagulacioni odgovor na
terapiju.
Chart 1. Anticoagulation response on therapy.
Starost i polna struktura nisu značajno uticali na kvalitet
antikoagulacije (Tabela 3). Srednja vrednost CHA2DS2-VASc skor-a za
rizik tromboembolizma je bila nešto viša u grupi C (A=3,3, vs B=3,4
Vs C=3,6 ) ali bez statističke razlike, dok je srednja vrednost
rizika od krvavljenja HASBLED skora bila nešto niža u grupi C ali
bez statističke razlike. Međutim u individualnoj distribuciji, broj
osoba sa povišenim rizikom za krvarenje (HAS-BLED>3) bio je
statistički značajno najniži u grupi C sa slabim kvalitetom
antikoagulacije (A 28,6% vs B=32% vs C22,6%, p<0,05).
Srednja vrednost indeksa telesne mase (BMI) je bila nešto niža u
grupi A (29,8 kg/m2) ali bez statističke razlike u odnosu na grupe B
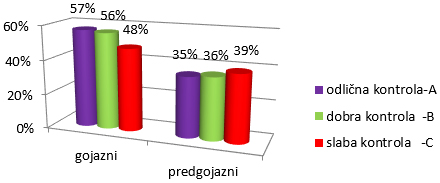
i C (30,9 kg/m2 identično). U individualnoj distribuciji (Grafikon
3) u sve tri grupe dominiraju gojazni bolesnici (A-57%, B-56%,
C-48%) i predgojazni (A-35%, B-36%, C-39%) bez statistički značajne
razlike. (Xi²= 0.487, NS).
Grafikon 2. Uticaj BMI na efekat
antikoagulacione terapije.
Chart 2. Influence of BMI on the effect of anticoagulation
therapy.
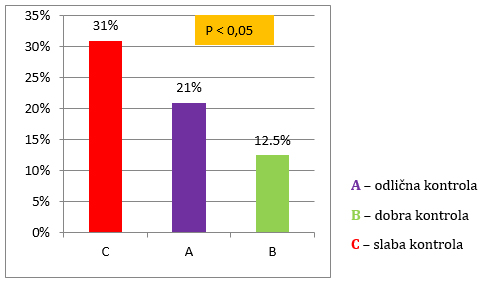
Najviši nivo glikemije je bio u grupi C sa slabim kvalitetom
antikoagulacije (C-6,5 versus A i C=5,8mmol/L) gde je bilo i
statistički značajno više dijabetičara (C=31% versus A-21% vs B 12,5
%). (Grafikon 3)
Grafikon 3. Uticaj prisustva Diabetes
mellitus tip 2 efekat antikoagulacione terapije.
Chart 3. Influence of Diabetes mellitus typ 2 presence on the
effect of anticoagulation therapy.
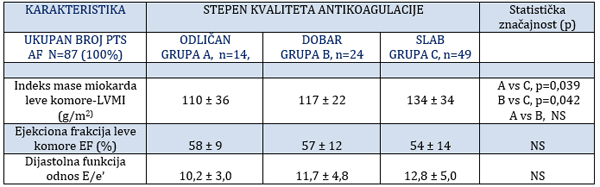
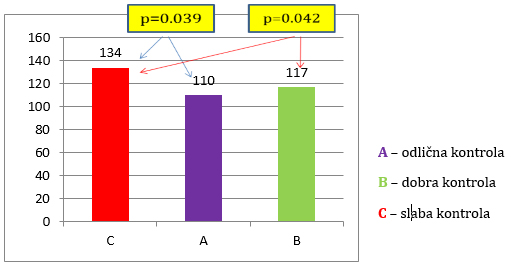
Analizom ehokardiografskih parametara (Tabela 5) utvrđeno je da
ne postoji statistički značna razlika u parametrima sistolne i
dijastolne funkcije među ispitivanim grupama. Jedino je nađen
statistički značajno viši indeks mase miokarda (LVMI) koji
reprezentuje stepen hipertrofije miokarda leve komore u grupi C-sa
slabim kvalitetom antikoagualcije u odnosu na grupe A i B
(C-LVMI=134g/m2 vs A =110; A vs C, p=0,039; B=117 g/m2, B vs C
(p=0,042) što je prikazano na Grafikonu 4.
Tabela 5. Ehokardiograski parametri kod 87
pacijenata podeljenih u 3 grupe prema kvalitetu antikoagulantne
terapije
Table 5. Echocardiographic parameters of 87 patients divided
in 3 groups according to quality of anticoagulation therapy
Grafikon 4. Analiza ehokardiografskih
parametara mase miokarda leve komore.
Chart 4. Analysis of echocardiographic parameters which
reprezenting left ventricular myocardial mass.
DISKUSIJA
S obzirom da postoje dokazi da vođenje oralne antikoagulantne
terapije (OAKT) striktno po vodiču dovodi do poboljšanja ishoda,
jako je važno inistirati na kvalitetu antikoagulacije uz maksimalnu
participaciju pacijenta, koji je adekvatno edukovan [16, 17].
Posebno je važno ne podceniti pacijente koji imaju samo jedan rizik
faktor za moždani udar, (CHA2DS2-VASc skor = 1) pošto opservacioni
podaci kohortnih studija iz "stvarnog života - real world life"
pokazuju da takvi pacijenti imaju više moždanih udara, sistemskih
embolizacija i veći mortalitet u odnosu na one sa uvedenom OAKT
[18]. Ipak zbog superiornosti Ne-vitamin-K-oralnih antikoagulansa
(NOAK-a) u odnosu na antagoniste vitamina K (VKA), posebno zato što
daju stalno optimalnu antikoagulaciju bez potrebe podešavanja doze,
NOAK lekovi treba da budu prva linija antitrombotskog tretmana kod
većine pacijenata sa AF koji imaju jedan dodatni rizik faktor za
možadani udar [18].
Vreme u terapijskom opsegu (TTR) nije moglo da se izračuna kod
većine ispitanika najčešće korišćenom metodom Rosendaala [14], jer
nisu imali dovoljno veliki broj merenja INR u toku godina dana (12
odnosno jednom mesečno) kao ni alternativnom metodom iz ROCKET AF
studije [15]. Zato je kreirana i korišćena naša orginalna klinička
aproksimacija na bazi kliničkih kriterijuma za kvalitet
antikoagulacije. Kriterijum za odličnu antikoagulisanost je bio da u
toku godinu dana 5 do 7 izmerenih vrednosti PT/INR bude ≥ 2
(analogno vremenu u terapijskom opsegu -TTR >60-85% vremena). Dobra
antikoagulisanost je definisana da 3 do 4 vrednosti PT /INR budu u
terapijskom opsegu (analogno TTR 50 do 60% vremena) dok je slaba
antikoagulisanost: 0-2 izmerene vrednosti INR u terapijskom opsegu
(TTR <50%). Ova metoda procene ima mana ali je jedini mogući
aproksimativni metod u svakodnevnoj praksi, dok bolesnici ne shvate
značaj redovnog određivanja efekta OAKT putem merenja PT/INR jednom
mesečno ili češće u slučaju nepostizanja ciljnih vrednosti od 2,0 do
3,0.
Standardni TTR, mera kontrole dikumarolske antikoagulacije, zavisi
od uticaja dnevnih vraijacija INR vrednosti većine dana praćenja
[14]. Zato je preporuka da se vreme u terapijskom opsegu (TTR)
izračunava po metodi ROCKET AF studije koja bolje reflektuje uticaj
na promenu doze leka nego Rosendaal metod [15]. Naša orginalna i
jednostavna metoda pogodna je za brzu orijentaciju u svakodnevnoj
praksi ali ipak treba da se evaluira na većem broju ispitanika i
dužim praćenjem.
U toku praćenja od godinu dana, na osnovu sukcesivnih vrednosti
PT/INR ukupno 87 bolesnika sa atrijalnom fibrilacijom 38 bolesnika
ili 44% je imalo relativno dobar kvalitet antikoagulacije. Najmanja
Grupa A je imala odličan kvalitet antikoagulantnog efekta N=14/87
(16%). U Grupi B kvalitet antikoagulacije je bio dobar u 24
bolesnika ili 28%. Najveća grupa C od 49 bolesnika (56%) imala je
slab kvalitet antikoagulantnog efekta sa visokim rizikom za
tromboembolijske komplikacije. Nelson WW i saradnici [19] su u
velikoj studiji za 12 meseci praćenja na oko 23000 pacijenata našli
srednji TTR=67%, sa samo 19% pacijenata koji su imali slab kvalitet
antikogulacije. Upoređivanjem naših podataka sa ovom velikom
studijom, 56% naših pacijenata ili 2,9 puta više ima slab kvalitet
antikoagulacije. Naši pacijenti ne kontrolišu PT/INR dovoljno često,
obično na 1,5 do 2 meseca, pa zato i nemaju šansu da se postignu
ciljne vrednosti INR titriranjem doze VKA. Unos hrane koja sadrži
visok nivo vitamina K takođe je doprinoseći faktor. Nelson WW i
saradnici [19] su logističkom regresionom analizom određivali
udruženost komorbiditeta i TTR. Oni nalaze da su faktori udruženi sa
slabim kvalitetom antikoagulacije: hipertenzija (41,7%), dijabetes
mellitus tip 2 (24,1%), srčana insuificijencija (11,7%) i predhodni
moždani udar (11,1%). Mi ne nalazimo povezanost lošeg kvaliteta
antikoagulacije sa hipertenzijom i srčanom insuficijencijom, ali u
našem istraživanju dijabetes mellitus tip 2 je najvažniji
komorbiditet, statistički značajno udružen sa slabom koagulacijom.
Podgrupa C ima čak 31 % dijabetičara prema 24% u studiji Nelsona WW
i saradnika (C=31% versus A-21% vs B 12,5 %). Hong KS i saradnici
[20] u studiji objavljenoj 2017 godine u 16 Korejanskih centara na
1230 bolesnika sa AF i predhodnim moždanim udarom, praćenjem oko 27
meseci našli su srednji TTR 49,1%. Ni jedan od ovih centara nije
postigao TTR>60% kao terapijski cilj [20]. Čak 42% su imali slab
kvalitet antikoagulacije (a već su preležali moždani udar) dok je u
našoj studiji sa slabim kvalitetom bio nešto veći broj bolesnika
(56%) ali je bilo samo 6,9% pacijernata sa možadnim udarom.
Iranska studija Frasada BF i saradnika [21] objavljije srednju
vrednost TTR=55% a slab kvalitet antikoagulacije ima 38% pacijenata.
Jedini su proučavali uticaj ko-medikacije na INR i našli da je
prediktor slabog kvaliteta antikoagulacije konkurentna upotreba više
od 4 leka (OR=2,06)
Melamed OC i saradanici [22] jednogodišnjim praćenjem na 906
pacijenata nalaze slab kvalitet antikoagulisanosti grubo u 2/3 (66%)
ispitanika. Srednji TTR je bio 48,6%. Oni nalaze da je slab
kvaliteta antikoagulacije povezan sa ženskim polom, odmaklom
starošću pacijenata i komorbiditetima. Od komorbiditeta srčana
insuficijencija povezana je sa slabim kvalitetom antikoagulacije
(OR=1,63), dok nema statistički značajne povezanosti sa dijabetesom
što se razlikuje od naših podataka. Takođe nema uticaja hipertenzije
na slab kvalitet antikoagulacije, saglasno sa našom studijom a što
je suprotno studiji Nelsona WW i saradnika [19]. Melamed OC i
saradnici [20] takođe uključuju i neadekvatnost lekara u vođenju
OAKT terapije kao važan faktor u slabom kvalitetu antikoagulacije
(bez sertifikata za vođenje OAKT, OR=1,41).
U najvećoj studiji na 34346 bolesnika sa AF i novouvedenim
varfarinom [23] nađeno je da vrednosti INR<2,0 dovode do povećanog
relativnog rizika ne samo za tromboembolijske komplikacije TIA
(relativni rizik RR=8) i ishemični moždani udar (RR=7,6) već i za
akutni koronarni sindrom (RR=7,9) [23].
AuriculA, veliki švedski nacionalni registar za atrijalnu
fibrilaciju i antikoagulaciju [24] korišćen je za procenu doziranja
VKA i kvalitet antikoagulacije putem TTR na 18391 sa AF. Oni su
dobili jedne od najboljih rezultata uopšte u svetu sa srednjim TTR
od 76,2%, što je mnogo više nego u pomenutim prospektivnim i
randomizovanim studijama i registrima. Frekvenca tromboembolijskih
komplikacija i velikih krvarenja je bila niska, respektivno 1,7% i
2,6% na godinu lečenja. Nije nađena korelacija između
tromboembolijskih komplikacija i starosti pacijenata, kao što su to
našli Melamed OC i saradanici [22], već sa velikim krvarenjima.
Korišćenje AuriculA programa doziranja VKA može da posluži za
obrazac postizanja dobre antikoagulisanosti za druge ustanove koje
se bave ovim problemom [24]. U najveću meta-analizu studija sa VKA u
AF analizom baza podataka MEDLINE, CENTRAL and EMBASE godine
uključeno je 68 studija od 1990-2013 godine [25]. Pacijenti su
proveli 61% vremena u terapijskom opsegu INR (TTR) dok je 25% imalo
slab kvalitet antikoagulacije a 14% je bilo sa INR iznad>3,0. Oko
57% tromboembolijskih komplikacija se desilo kod INR<2,0 a 42%
hemoragijskih komplikacija kod INR >3,0. Pacijenti na VKA u AF često
imaju INR van terapijskog ranga. Dok se tromboembolijski i
hemoragijski događaji nažalost dešavaju i u pacijenata u terapijskom
opsegu 2,0 do 3,0, ipak pacijenti sa INR<2,0 čine većinu pacijenata
sa tromboembolizom. Analogno tome pacijenti sa INR>3,0 čini najveći
broj sa hemoragijom. Vođenje OAKT van kliničkih studija ili van
bolnica je udruženo sa slabijim kvalitetom antikoagulacije, posebno
u periodu pri uvođenju OAKT. Pacijenti u Evropi imaju bolju kontrolu
INR nego u Severnoj Americi. Antagonisti vitamina K (VKA) su
efektivni oralni antikoagulantni lekovi koji se titriraju do
dostizanja uskog terapijskog ranga od INR 2-3. što je nekada teško
postići [24]. Vreme u terapijskom opsegu TTR od ≥65 % je uobičajeno
prihvaćeno kao definicija stabilnosti INR [26]. Postoji heterogenost
u podacima vezanim za kvalitet OAKT u pogledu definicije za odličan,
dobar i slab kvalitet antikoagulacije. U našoj studiji mi smo
koristili načešče koriščen kriterijum TTR ≥60 % [20] dok neki autori
smatraju da je to ≥65 % [26] ili ≥70% [24]. U stvarnom životu, van
studija, retko se postižu ovi standardi što povećava mogućnost
tromboembolijskih komplikacija i velikih krvarenja. Postoje jaki
dokazi da je apsolutni benefit od OAKT veći što je veći
tromboemboliski rizik prema CHA2DS2-VASc skoru, pa u celom kontekstu
NOAK lekovi imaju veći klinički benefit u poređenju sa VKA posebno u
najrizičnijih pacijenata [10, 11, 27].
Postizanje odličnog kvaliteta antikoagulacije mora biti zadatak u
svih booesnika sa AF i CH2DS2-VASc skorom 2 i više (nekad i 1)
posebno u najrizičnijim podgrupama bolesnika sa atrijalnom
fibrilacijom i komorbiditetima: dijabetičarima, hipertenzivnim
pacijentima sa srčanom insuificijencijom i preležanim moždanim
udarom i TIA [2, 19].
CH2DS2-VASc skor (rizik tromboembolizma) je bio nešto viši u grupi C
(A=3,3, vs B=3,4 Vs C=3,6) dok je rizik od krvavljenja HAS-BLED
skor>3 bio u individualnoj distribuciji statistički značajno niži u
grupi C (B=32% vs A 28,6% vs C22,6. U literaturi nismo našli da je
neko radio ovake komparacije ali je logičan nalaz pošto veći rizik
prema CH2DS2-VASc nosi teže postizanje ciljnog INR.
Gojaznost i predgojaznost je dominirala u individualnoj distribuciji
u sve tri grupe ali bez statistički znčajne povezanosti sa
kvalitetom antikoagulacije, što je u skladu sa podacima iz
literature. Jedino može da se konstatuje da je metabolički sindrom
češće udružen sa atrijalnom fibrilacijom, ali bez upliva na stepen
kvaliteta antikoagulacije što je nedavno pokazano u studiji Raščanin
A. i saradnici [28].
U dostupnoj literaturi do sada niko nije analizirao udruženost
ehokardiografskih parametara sa kvalitetom antikoagulantnog efekta
OAKT. U našoj studiji dobijen je statistički značajno viši indeks
mase miokarda (LVMI) u grupi C sa slabim kvalitetom antikoagulacije
-C-LVMI=134 g/m2 vs A =110 vs B 117 (A vs C, p=0,039; B vs C
(p=0,042), ali nismo našli povezanost sa srednjim vrednostima
sistolnog i dijastolnog krvnog pritiska. Ovo se može objasniti
predpostavkom da ti pacijenti sa hipertrofijom miokarda u sklopu
hipertenzivnog srca i slabim kvalitetom antikoagulacije imaju duže
trajanje i teži stepen hipertenzije što bi trebalo posebno
istraživati. Udruženost hipertenzije i slabog kvaliteta
antikoagulacije je dokazana u velikim studija [19].
Mnogo faktora je udruženo sa slabom kontrolom INR, odnosno slabim
kvalitetom antikoagulacije: Pacijenti lečeni ambulantno; oni sa
novouvedenim VKA; mlađi i stariji odmakle dobi; nekomplijantni za
terapiju i merenje INR; nepridržavanje saveta o izbegavanju hrane
bogate vitaminom K; Uzimanje više od 4 leka uz OAKT; Nivo edukacije
lekara primarne i sekundrane zdravstvene zaštite; Takođe multipli
organski i mentalni komorbiditeti su udruženi sa nižim TTR najčešće
hipertenzija, dijabetes melitus, srčana insuficijencija. Ipak jedan
od najvažnijih faktora su genetski faktori [26]. Klinički prediktori
su dostupni za analizu ali oni mogu objasniti ipak samo 10%
varijanse koja leži iza loše kontrole INR. Zato genetski faktori
polimorfizam CYP2C9 i/ili VKORC1 i neki drugi geni imaju veliki udeo
u slabom kvalitetu antokoagulacije [26].
Kao što se vidi iz svega gore navedenog u literaturi postoji
heterogenost u podacima vezanim za kvalitet antikogulantne terapije
i rizik faktore i prediktore slabog kvaliteta antikoagulacije. Razne
studije analiziraju različite grupe faktora, jedne uzimaju manji a
druge veći broj rizik faktora i prediktora te ne postoji
konzistentnost u ovakvima nalaizama. Bilo bi poželjno da velike
propsektivne studije urade sveobuhvatno praćenje ovih fakora. Lekari
treba da ohrabre pacijente da intenziviraju marljivost u redovnom
uzimanju leka i kontroli INR kada koriste antagoniste vitamina K
(VKA) i da razmotre prelazak na nove antikoagulantne, Ne-Vitamin-K
antagoniste u prvom redu dabigatran i rivaroksaban kao terapijske
opcije u bolesnika sa AF gde je labilan INR ili loša komlijansa u
kontroli INR [10, 11, 26, 27].
ZAKLJUČAK
Odličan i dobar kvalitet antokoagulantnog efekta hronične
terapije antagonistima vitamina K u cilju prevencije tromboembolizma
je u toku jednogodišnjeg praćenja bio samo kod 44% bolesnika.
Nažalost dominira slab kvalitet antikoagulacije kod čak 56%
bolesnika. Od kliničkih faktora koji su povezani sa slabim
antikoagulantnim efektom značajni su prisustvo hiperglikemije i
dijabeta. Ehokardiografski određena težina hipertrofiie leve komore
je statistički značajno povezana sa slabim antikoagulantnim efektom.
Klinički prediktori su lako dostupni za analizu ali oni mogu
objasniti ipak samo 10% varijanse koja leži iza loše kontrole INR.
Zato genetski faktori polimorfizam CYP2C9 i/ili VKORC1 imaju veliki
udeo u slabom kvalitetu antokoagulacije. Glavni razlog za slabiji
kvalitet antikoagulacije, u odnosu na zemlje zapadne Evrope uz
genetske faktora jeste loša komplijansa pacijenata.
LITERATURA
- Olesen JB, Lip GY, Hansen ML, Hansen PR, Tolstrup JS,
Lindhardsen J. Validation of risk stratification schemes for
predicting stroke and thromoembolism in patients with atrial
fibrillation: nationwide cohort study. BMJ 2011;342:d124.
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei
B. et al. 2016 ESC Guidelines for the management of atrial
fibrillation developed in collaboration with EACTS. European
Heart Journal 2016; 37: 2893–2962.
- Potpara TS, Lip GY. Oral anticoagulant therapy in atrial
fibrillation patients at high stroke and bleeding risk. Prog
Cardiovasc Dis. 2015; 58(2):177-194.
- Quinn GR, Severdija ON, Chang Y, and Singer DE. Contemporary
Trends in Oral Anticoagulant Prescription in Atrial Fibrillation
Patients at Low to Moderate Risk of Stroke After
Guideline-Recommended Change in Use of the CHADS to the Wide
Variation in Reported Rates of Stroke Across Cohorts of Patients
With Atrial Fibrillation.Circulation. 2017; 135(3):208-219.
- Allan V, Banerjee A, Shah AD, Patel R, Denaxas S, Casas JP,
Hemingway H. Net clinical benefit of warfarin in individuals
with atrial fibrillation across stroke risk and across primary
and secondary care. Heart. 2017; 103(3): 210-218.
- Ageno W, Gallus AS, Wittkowsky A, Crowther M, Hylek EM,
Palareti G. Oral anticoagulant therapy: antithrombotic therapy
and prevention of thrombosis, American College of Chest
Physicians evidence-based clinical practice guidelines. Chest.
2012; 141 (suppl 2):e44S–e88S.
- Dlott JS, George RA, Huang X, Odeh M, Kaufman HW, Ansell J,
Hylek EM. National assessment of warfarin anticoagulation
therapy for stroke prevention in atrial fibrillation.
Circulation. 2014; 129: 1407–1414.
- Katz DF, Maddox TM, Turakhia M, Gehi A, O'Brien EC, Lubitz
SA, et al. CHA2 DS2 -VASc Score for Thrombo-embolic Risk
Assessment: Analysis From the National Cardiovascular Data
Registry's Outpatient Practice Innovation and Clinical
Excellence Atrial Fibrillation Registry. Circ Cardiovasc Qual
Outcomes. 2017;10(5). Available from: pii: e003476. doi:
10.1161/ CIRCOUTCOMES. 116.003476.PMID: 28506981
- Mazurek M, Shantsila E, Lane DA, Wolff A, Proietti M, Lip
GYH. Guideline-Adherent Antithrombotic Treatment Improves
Outcomes in Patients With Atrial Fibrillation: Insights From the
Community-Based Darlington Atrial Fibrillation Registry. Mayo
Clin Proc. 2017; 92: 1203-1213.
- Zirlik AJ, Bode C Vitamin K antagonists: relative strengths
and weaknesses vs. direct oral anticoagulants for stroke
prevention in patients with atrial fibrillation. Thromb
Thrombolysis. 2017; 43(3):365-379.
- Chen ST, Patel MR. Comparison of anticoagulant therapy for
atrial fibrillation -novel oral anticoagulants versus vitamin K
antagonists. Prog Cardiovasc Dis. 2018 Jan 12. pii:S0033-0620
(18)30024-0. doi: 10.1016/j.pcad. 2018.01.005. Epub 2018 Jan 12.
- Brandes A, Overgaard M, Plauborg L, Dehlendorff C, Lyck F,
Peulicke J et al Guideline adherence of antithrombotic treatment
initiated by general practitioners in patients with nonvalvular
atrial fibrillation: a Danish survey. Clin Cardiol.
2013;36:427-32.
- Pisters R, Lane DA, Nieuwlaat R, De Vos CB.; Crijns HJ, Lip
GY. Novel User-Friendly Score (HAS-BLED) to Assess 1-Year Risk
of Major Bleeding in Patients with Atrial Fibrillation. Chest
2010; 138: 1093–1100.
- Rosendaal FR, Cannegieter SC, Van der Meer FJ, Briet E. A
method to determine the optimal intensity of oral anticoagulant
therapy. Thromb Haemost.1993;69:236–239.
- Singer DE, Hellkamp AS, Yuan Z, Lokhnygina Y, Patel MR.
Alternative Calculations of Individual Patient Time in
Therapeutic Range While Taking Warfarin: Results From the ROCKET
AF Trial. J Am Heart Assoc. 2015;4: Available from: e001349 doi:
10.1161/JAHA. 114.001349)
- Lip GY, Laroche C, Popescu MI, Rasmussen LH, Vitali-Serdoz
L, et al. Improved outcomes with European Society of Cardiology
guideline-adherent antithrombotic treatment in highrisk patients
with atrial fibrillation: a report from the EORP-AF General
Pilot Registry. Europace. 2015; 17: 1777-1786.
- Proietti M, Nobili A, Raparelli V, Napoleone L, Mannucci PM,
Lip GY; Adherence to antithrombotic therapy guidelines improves
mortality among elderly patients with atrial fibrillation:
insights from the REPOSI study. Clin Res Cardiol. 2016; 105:
912-920.
- Potpara TS, Dagres N, MujovicN, Vasic D, Asanin M, Lip GYH.
Decision-Making in Clinical Practice: Oral Anticoagulant Therapy
in Patients with Non-valvular Atrial Fibrillation and a Single
Additional Stroke Risk Factor. Adv Ther 2017; 34: 357–377
- Nelson WW, Choi JC, Vanderpoel J. Impact of Co-morbidities
and Patient Characteristics on International Normalized Ratio
Control Over Time in Patients With Nonvalvular Atrial
Fibrillation. Am J Cardiol 2013; 112: 509-512.
- Hong KS, Kim YK, Bae HJ, Nam HS, Kwon SU, Bang OY et al.
Quality of Anticoagulation with Warfarin in Korean Patients with
Atrial Fibrillation and Prior Stroke: A Multicenter
Retrospective Observational Study. J Clin Neurol 2017; 13(3):
273-280.
- Farsad BF, Abbasinazari M, Dabagh A. Bakshandeh H.
Evaluation of Time in Therapeutic Range(TTR) in Patients with
Non-Valvular Atrial Fibrillation Receiving Treatment with
Warfarin in Tehran, Iran: A Cross-Sectional Study.Journal of
Clinical and Diagnostic Research. 2016; 10(9): FC04-FC06.
- Melamed OC , Horowitz G, Elhayany A, Vinker S. Quality of
anticoagulation control among patients with atrial fibrillation.
Am J Manag Care. 2011; 17(3): 232-237.
- Nelson WW, Wang L., Baser O. Damaraju CV, Schein JR.
Out-of-range INR values and outcomes among new warfarin patients
with non-valvular atrial fibrillation. Int J Clin Pharm 2015;
37: 53–59.
- Wieloch M, Själander A, Frykman V, Rosenqvist M, Eriksson N,
Svensson PJ. Anticoagulation control in Sweden: reports of time
in therapeutic range, major bleeding, and thrombo-embolic
complications from the national quality registry AuriculA. Eur
Heart J. 2011; 32(18): 2282-2289.
- Mearns ES, White CM, Kohn CG, Hawthorne J, Song JS, Meng J.
Quality of vitamin K antagonist control and outcomes in atrial
fibrillation patients: a meta-analysis and meta-regression.
Thrombosis Journal 2014;2:14 Available from:
http://www.thrombosisjournal.com/content/12/1/14
- Schein JR, White CM, Nelson WW , Kluger J , Mearns ES ,
Coleman CI . Vitamin K antagonist use: evidence of the
difficulty of achieving and maintaining target INR range and
subsequent consequences. Thrombosis Journal. 2016 Jun 13; 14:
14. Available from: http://www.thrombosisjournal.com/
content/12/1/14doi:10.1186/s12959-016-0088-y. eCollection 2016.
DOI 10.1186/s12959-016-0088-y
- Potpara TS, Lip GY. Oral anticoagulant therapy in atrial
fibrillation patients at high stroke and bleeding risk. Prog
Cardiovasc Dis.2015; 58(2):177-94.
- Raščanin A, Aranđelović I, Bastać M, Bastać D. Uticaj
metaboličkog sindroma na strukturne anomalije, sistolnu i
dijastolnu funkciju leve komore određivanu ehokardiografijom u
bolesnika sa atrijalnom fibrilacijom. Timočki medicinski glasnik
2017; 42(3): 132-138.
|
|
|
|









