|
|
|
|
UVOD Dislipidemije
obuhvataju poremećaje metabolizma lipida koji značajno doprinose
razvoju aterosklerotske kardiovaskularne bolesti (ASKV). Povišen
holesterola lipoproteina niske gustine LDL-C predstavlja glavni
uzročni faktor aterogeneze. Dislipidemije predstavljaju heterogenu
grupu poremećaja metabolizma lipida koje karakterišu povišene ili
snižene koncentracije lipoproteina u plazmi. One su ključni,
modifikabilni faktor rizika za aterosklerotsku kardiovaskularnu
bolest (ASCVD), uključujući koronarnu bolest srca, cerebrovaskularna
oboljenja i periferne vaskularne bolesti. Epidemiološki podaci
pokazuju jasnu linearnu vezu između nivoa LDL holesterola (LDL-C) i
učestalosti kardiovaskularnih događaja, potvrđujući LDL-C kao
primarni uzročni faktor aterogeneze [1–7].
Kod očigledno zdravih osoba, rizik za nastanak ASKVB je najčešće
rezultat interakcije višestrukih faktora rizika. Ovo je osnova za
procenu i upravljanje ukupnim KV rizikom. Kod skrininga faktora
rizika morali bi obuhvatiti i lipidni status kod muškaraca >40
godina starosti i kod žena >50 godina starosti ili nakon menopauze.
Osavremenjeni elektronski internet Sistem za procenu rizika Heart
Score (www.heartscore.org): SCORE 2 i SCORE 2OP doprinosi kod
donošenja logičnih odluka u lečenju da bi se izbeglo subdoziranje
ili predoziranje hipolipemicima. Određene osobe prezentovane sa
visokim ili veoma visokim ili ekstremnim rizikom za razvoj KVB ne
zahtevaju procenu rizika, već hitno zbrinjavanje svih faktora
rizika. Ovo važi za pacijente sa dokazanom ASKVB, dijabetes
mellitusom (DM) ili hroničnom bubrežnom bolešću (HBB) stadijuma veće
od G3b-4 ili manifestnom hroničnom bubrežnom insuficijencijom (HBI).
Mora se napomenuti da su svi sistemi za procenu rizika prilično
kruti i zahtevaju dodatnu pažnju prilikom kreiranja završnog stava u
lečenju. Dodatni faktori koji utiču na procenu rizika svrstani su u
elektronskom sistemu za procenu kao što je Heart Score
(www.heartscore.org). Pristup ukupnoj proceni rizika dozvoljava
fleksibilnost, ukoliko se ne može dostići najbolji preventivni
rezultat sa jednim faktorom rizika, rizik se svakako može sniziti sa
jačim delovanjem na ostale faktore rizika.
Prema aktuelnim svetskim, američkim i evropskim smernicama sve
srpske nazive ADA, AHA/ACC, ESC/EAS 2023–2026), rana dijagnostika i
agresivna kontrola lipidnog profila ostaju centralne komponente
prevencije ASCVD. [3–5].
U periodu 2023.–2026. godine objavljene su nove verzije ključnih
međunarodnih smernica za lečenje dislipidemija, uključujući:
Evropsko kardiološko i Evropsko aterosklerotsko društvo (ESC/EAS),
Američko udruženje za srce(AHA), Američki koledž kardiologa (ACC) i
Američko udruženje za dijabetes (ADA).
Sve ove smernice ističu potrebu za ranijom, intenzivnijom i
kombinovanom terapijom radi postizanja što nižih vrednosti
aterogenih lipoproteina, sa posebnim fokusom na LDL-C, non-HDL-C i
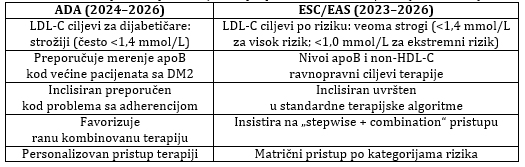
apolipoprotein B (apoB) [3–5] (Tabela 1).
Tabela 1. Uporedni prikaz ključnih preporuka ADA vs ESC/EAS
(2023–2026)
CILJ RADA
Cilj ovog preglednog rada je da sveobuhvatno prikaže savremene
principe dijagnostike, klasifikacije ranog skrininga, procene
desetogodišnjeg kardiovaskularnog rizika SCORE 2 i SCORE 2OP alatima
i terapijskog upravljanja dislipidemijama u skladu sa najnovijim
međunarodnim standardima prema aktuelnim smernicama i vodličima
(ESC,EAC, ADA, AHA, ACC).
KLASIFIKACIJA DISLIPIDEMIJA
Primarne dislipidemije
• Porodična hiperholesterolemija (FH)
• Familijarna kombinovana hiperlipidemija
• Poligenska hiperlipidemija
Sekundarne dislipidemije
Najčešće uzrokovane:
• dijabetes melitus,
• gojaznost i metabolički sindrom,
• hronična bubrežna bolest,
• hipotireoza,
• bolesti jetre,
• lekovi (kortikosteroidi, antipsihotici, retinoidi,
imunokompresivi) [15–17].
DIJAGNOZA DISLIPIDEMIJA
Standardni dijagnostički pristup
Dijagnostika uključuje merenje standardnog lipidnog profila: ukupni
holesterol, LDL-C, HDL-C, trigliceridi; izračunavanje non-HDL-C i
apoB; procenu sekundarnih uzroka; procenu globalnog
kardiovaskularnog rizika i ispitivanje porodične anamneze.
Skrining za dislipidemiju je uvek indikovan kod pacijenata sa
kliničkim manifestacijama KVB, u kliničkim stanjima povećanog KV
rizik i kad god se ukaže potreba za skriningom faktora rizika. U
nekoliko kliničkih stanja, dislipidemija može doprineti povećanju
rizika za razvoj KVB. Autoimuna hronična inflamatorna stanja kao što
su reumatoidni artritis, sistemski lupus eritematosus (SLE) i
psorijaza se smatraju stanjima u kojima je povećan KV rizik. Pored
toga, kod žena, dijabetes i hipertenzija tokom trudnoće su rizični
indikatori, a kod muškaraca, erektilna disfunkcija. Pacijenti sa
hroničnom bubrežnom bolešću i manifestnom bubrežnom insuficijencijom
takođe imaju uvećan KV rizik i kod njih je indikovan skrining za
dislipidemiju.
Uvek je potrebno identifikovati kiničke manifestacije genetskih
dislipidemija, kao što su ksantomi, ksantelazme i rani arcus
cornealis (pre 45 godina), jer su oni indikatori ozbiljne
lipoproteinske bolest, pre svega porodične hiperholesterolemije
(FH), koja je najčešće uzrok monogenetskih poremećaja i udružena je
sa preranom ASKVB. Skrining za dislipidemiju je takođe indikovan kod
pacijenata sa perifernom arterijskom bolešću (PAB) ili u prisustvu
povećanja debljine intima-medija karotida (IMK) ili karotidnih
plakova.
Skrining za dislipidemiju bi trebalo razmotriti kod svih odraslih
muškaraca ≥40 godina ili kod žena ≥50 godina ili u ranoj
postmenopauzi, posebno u prisustvu ostalih faktora rizika. Takođe,
je indikovano za skrining potomaka pacijenata sa ozbiljnom
dislipidemijom i njihovo praćenje u specijalizovanim klinikama, ako
je potrebno. Takođe, preporučuje se skrining i članova porodica
pacijenata sa preuranjenim ASKVB [2].
Evaluacija laboratorijskih parametara lipida i apolipoproteina [2]
Predložene analize koje se koriste za procenu lipida su ukupni
holesterol (TC), trigliceridi (TG), HDL-C, LDL-C. Uzorci krvi uzeti
nakon gladovanja i oni nakon obroka daju slične rezultate za totalni
holesterol (TC), LDL-holesterol i HDL-holesterol. Trigliceridi (TGs)
su uslovljeni hranom. Postoji značajna unutar-pojedinačna varijacija
kod serumskih lipida. Varijacije od 5-10% za TC i >20% za TG,
posebno kod pacijenata sa hipertrigliceridemijom (HTG), nisu
retkost. Ovo je donekle zbog analitičke varijacije, ali je takođe i
zbog spoljnih faktora poput ishrane, intenziteta fizičke aktivnost,
i sezonskih varijacija poput povišenog nivoa TC i HDL-holesterola
tokom zime.
LDL holesterol - U većini kliničkih studija LDL-holesterol je
izračunat pomoću Friedewald-ove formule [2]:
LDL-C =TC -HDL-C - TG/ 2.2; u mmol/L
LDL-C = TC - HDL-C - TG/5 u mg/dL
Metodološke greške se mogu akumulirati jer se oslanjaju na 3
analize: za ukupni holesterol (TC), trigliceride (TGs) i
HDL-holesterol. Direktne metode za određivanje LDL-holesterola su
dostupne i one se sada široko koriste. Generalno, direktne i
indirektne (izračunate) vrednosti LDL-holesterola pokazuje dobro
slaganje. Nove formule za izračunavanje LDL-C kao što su
Martin/Hopkins, Sampson, posebno su preporučene u ADA i AHA/ACC
smernicama [3–4]. Direktne metode za utvrđivanje HDL–holesterola i
LDL–holesterola su trenutno široko korišćene i one su pouzdane kod
pacijenata sa normalnim vrednostima lipida. Međutim u
hipertrigliceridemiji (HTG) mogu biti nepouzdane, i rezultati mogu
varirati među komercijalnim testovima.
Lipoprotein(a)-LP(a) u nekoliko studija je pronađen kao dodatni
nezavisni faktor rizika; u patofiziologiji aterosklerotskih
vaskularnih bolesti i u aortnoj stenozi. LP(a) ima zajednička
svojstva sa LDL, ali on sadrži jedinstven protein, apolipoprotein
(a)-apo(a), koji je strukturno homolog plazminogenu. Merenja LP(a)
su posebno stabilna tokom vremena. Statini ne smanjuju nivo LP(a),
ali e smanjenje LP(a) za 30% prikazano upotrebom Proprotein
konvertaza subtilizin/keksin tip 9 (PCSK9) inhibitorima i
nikotinskom kiselinom. Uticaj na kardiovaskularne (CVD) događaje
koji ciljaju LP(a) gen nije dokazan. Lekovi koji utiču na Lp(a) gen
snižavaju nivoe ovih cirkulišućih proteina za preko 80%.
Najveći broj sistema za procenu KV rizika koriste TC i
LDL-holesterol, i upotreba ostalih mera, poput apoB, i
non-HDL-holesterola, mada deluje logično, zasnovani su na post hok
analizama. TC i LDL–C ostaju primarni ciljevi lečenja, dok
non-HDL-holesterol i apoB su identifikovani kao sekundarni ciljevi.
Kod pacijenta sa povišenim nivoom TG, dodatni rizik nose TG bogati
lipoproteini koji se moraju uzeti u obzir.
Totalni holesterol (TC) se preporučuje za procenu totalnog KV rizika
uz pomoć starog SCORE sistema. Međutim, u pojedinačnim slučajevima,
TC može biti obmanjujući. To se posebno odnosi na žene, koje često
imaju povišen nivo HDL-holesterola, i kod osoba obolelih od
dijabetesa ili sa povišenim vrednostima TG koji često imaju snižen
nivo HDL holesterola. Procena ukupnog rizika nije potrebna kod osoba
sa porodičnom hiperlipidemijom (uključujuči i FH) ili one sa TC
>7.5mmol/l (290mg/ml). Ovi pacijenti su uvek sa visokim rizikom i
trebalo bi im ukazati posebnu pažnju.
Non-HDL-holesterol se koristi za procenu totalnog iznosa aterogenih
lipoproteina u plazmi: VLDL, VLDL ostataka, holesterola srednje
gustine (IDL), LDL, Lp(a) i ima visoku korelaciju sa nivoima apoB.
Non-HDL-holesterol je lako izračunati:
non-HDL= TC – HDL-holesterol.
Prema updejtovanom vodiču ESC za dislipidemije [3] SCORE2 i SCORE2OP
preporučuju non-HDL-holesterol kao bolji indikator rizika od
LDL-holesterola. U nekoliko objavljenih analiza Sistema za procenu
rizika, non-HDL-holesterol je u odnosu na druge mere pokazao kao
superioran, dok u drugim, LDL-holesterol i non-HDL-holesterol daju
slične informacije. U poređenju sa non-HDL-holesterolom, korišćenje
LDL-holesterola u određenim situacijama ima prednosti. Non-HDL
holesterol se jednostavno izračunava i ne zahteva dodatne analize.
Non-HDL–holesterol takođe uključuje aterogene lipoproteine bogate
trigliceridima (VLDL, IDL i ostatke), koji su od suštinskog značaja
s obzirom na skorašnje informacije iz genetskih studija (GWASs) koje
podržavaju zapažanja da TG igraju značajnu ulogu u aterogenezi. Sva
dosadašnja istraživanja koriste LDL-holesterol, te je on primarni
cilj lečenja. Međutim, non-HDL holesterol bi trebalo koristiti kao
sekundarni cilj kada je LDL-ciljana vrednost dostignuta. Ciljana
vrednost za non-HDL-holesterol se lako izračunava kao zbir
LDL-holesterol ciljane vrednost na koju se doda 0.8 mm/L (30 mg/dL).
Lipoprotein visoke gustine – holesterol (HDL-holesterol)
Nizak HDL-holesterol se pokazao kao veoma značajan i nezavistan
faktor rizika u nekoliko studija i koristi se u većini Sistema za
procenu rizika, uključujući HeartScore. Veoma visoke vrednosti
HDL-holesterola nisu udružene sa ateroprotekcijom. Na osnovu
epidemioloških studija, nivo HDL-holesterola koji je asociran sa
povećanim rizikom je za muškarce < 1,0mmol/L (40mg/dL) i za žene <
1,2 mmol/L (48 mg/dL). Uloga HDL-holesterola za zaštitu protiv
kardiovaskularnih oboljenja (CVD) dovedena je u pitanje u nekoliko
studija koristeći Mendelian randomizaciju. Skorašnje studije ukazuju
da disfunkcionalni HDL može biti više relevantan za razvoj
ateroskleroze od nivoa HDL-holesterola.
Trigliceridi
Vrednosti triglicerida (TG) se određuju preciznim enzimskim
tehnikama. Retke greške se dešavaju kod pacijenata sa
hiperglicerolemijom, gde su detektovane greške kod veoma visokih
vrednosti TG. Visoki nivoi TG su često udruženi sa niskim
HDL-holesterolom i visokim nivoima LDL čestica male gustine. U
brojnim meta analizama TG mogu se pokazati kao nezavistan faktor
rizika. Pored toga, skoriji podaci o genetskim uzrocima podržavaju
tvrdnju da visoki nivoi TG direktno uzrokuju kardiovaskularne (CV)
bolesti. Skorašnje studije sugerišu da vrednosti TGs prilikom
ne-pošćenja mogu da nose informacije u pogledu lipoproteinskih
ostataka udruženih sa povećanim rizikom.
APOLIPOPROTEINI
Postoje dobre imunohemijske metode za odredjivanje apolipoproteina u
konvencionalnim autoanalizatorima. Analitička performansa je dobra i
analize ne zahtevaju uslove pošćenja i nisu osetljive na povišene
nivoe triglicerida (TG).
Apolipoprotein B (ApoB) je glavni apolipoprotein iz aterogenetske
porodice lipoproteina (VLDL, IDL i LDL). ApoB je dobar za procenu
velikog broja ovih čestica u plazmi. Ova karakteristika je veoma
važna u slučaju visoke koncentracije lipoproteina male gustine LDL.
Nekoliko prospektivnih studija je pokazalo je da apoB jednak
LDL-holesterolu i non-HDL-holesterolu prilikom predviđanja rizika.
ApoB nije ocenjen kao primarni cilj za lečenje u kliničkim
ispitivanjima, ali nekoliko post hok analiza kliničkih ispitivanja
predlaže da apoB može da se koristi ne samo kao marker rizika, već i
kao cilj lečenja.
Apolipoprotein A1. ApoA1 je glavni protein HDL-holesterola
i obezbeđuje zadovoljavajuće procene koncentracije HDL-holesterola.
Međutim, svaka čestica HDL može da nosi jednu do pet ApoA1 molekula.
Apolipoprotein CIII. Apo CIII je prepoznat kao potencijalno važan
novi faktor rizika. Apo CIII je ključni regulator za metabolizam TG
i visoki nivoi serumskog apo CIII su udruženi sa visokim nivoima
serumskih VLDL i serumskih TGs. Pored toga, gubitak funkcije
mutacijama je udružen sa niskim nivoima TG kao i sa smanjenim
rizikom za kardiovaskularne bolesti
Genetska dijagnostika [4]
Genetska dijagnostika se preporučuje kod sumnje na porodičnu
hiperholesterolemiju (FH), izuzetno visokih vrednosti LDL-C (>4,9
mmol/L ili >190 mg/dL) i porodične anamneze rane ishemijske bolesti
srca.
TERAPIJSKI PRISTUPI
Terapija dislipidemija zasniva se na kombinaciji nefarmakoloških i
farmakoloških strategija, usmerenih prvenstveno na redukciju LDL
holesterola, ali i na kontrolu triglicerida, povećanje HDL
holesterola i redukciju ukupnog aterogenog opterećenja. Savremene
smernice saglasne su u ključnom principu: “što niže – to bolje” u
odnosu na LDL C, posebno kod pacijenata sa visokim i veoma visokim
kardiovaskularnim rizikom [1–9].
1. Nefarmakološki pristupi
Modifikacija životnog stila - ovi pristupi predstavljaju osnovu
terapije kod svih pacijenata sa dislipidemijom, bez obzira na rizik.
Najvažnije intervencije obuhvataju redukcija unosa zasićenih i trans
masti; mediteranski ili DASH tip ishrane; povećanje unosa vlakana i
biljnih sterola; aerobna fizička aktivnost ≥150 min nedeljno;
redukcija telesne mase za ≥5–7% kod gojaznih pacijenata; prestanak
pušenja; redukcija alkohola kod hipertrigliceridemije. Iako promene
životnog stila smanjuju LDL C za 5–15%, kod pacijenata sa visokim
rizikom najčešće nisu dovoljne kao monoterapija [16–22].
2. Farmakološka terapija dislipidemija (Tabela 2 i Shema 1)
Tabela 2. Terapijske klase lekova — poređenje preporuka smernica
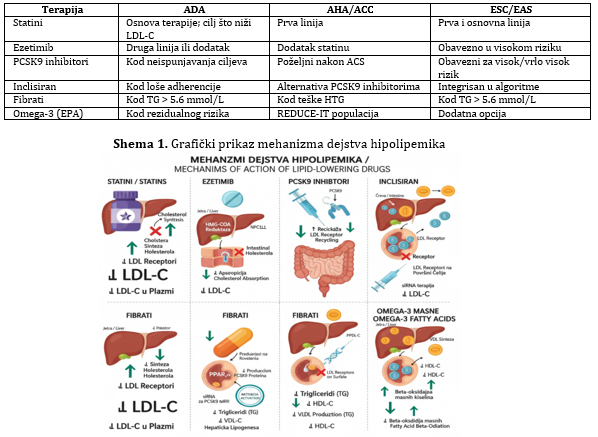
Statini (inhibitori HMG CoA reduktaze)
Statini su i dalje prva linija terapije kod većine pacijenata. Dele
se na: visokointenzivne (atorvastatin 40–80 mg, rosuvastatin 20–40
mg) i srednje intenzivne (simvastatin, pravastatin, lovastatin,
pitavastatin). Efekti su redukcija LDL C: 30–60% u zavisnosti od
doze i smanjenje rizika od infarkta miokarda, šloga i
kardiovaskularne (CV) smrti za 25–40% [8–10]. Nuspojave su
miopatije, povišenje jetrenih enzima, vrlo retko rabdomioliza.
Ezetimib (inhibitor apsorpcije holesterola)
Ezetimib inhibira NPC1L1 transporter u tankom crevu i time smanjuje
apsorpciju holesterola. Klinički značaj jeste da je preporučen kao
druga linija kod bolesnika kod kojih LDL C ostaje iznad cilja uz
maksimalnu dozu statina jer daje dodatnih 20–25% redukcije LDL C,
bezbedan je i dobro podnošljiv [13].
Proproteinska konvertaza subtilizin/keksin tip 9 (Proprotein
Convertase Subtilisin/Kexin Type 9) inhibitori ili PCSK9 inhibitori
su monoklonska antitela: Evolokumab i Alirokumab. Blokiraju PCSK9
protein, čime povećavaju recikliranje LDL receptora i obaraju LDL C
za 50–65%. Indikacije su pacijenti sa vrlo visokim rizikom
(preboleli infarkt, polivaskularna bolest); pacijenti sa FH;
bolesnici koji na maksimalnoj terapiji statinom + ezetimibom a ne
postižu ciljne vrednosti [10–11]. Velike studije (FOURIER, ODYSSEY
Outcomes) pokazale su značajno smanjenje KV mortaliteta i infarkta
miokarda.
Inklisiran (siRNA terapija)
Inklisiran je mala interferirajuća RNK (siRNA) koja blokira sintezu
PCSK9 u hepatocitima. Prednosti su da se primenjuje samo dva puta
godišnje i postiže se trajna redukcija LDL C od ~50% i da je idealan
za pacijente sa lošom adherencijom. Uključivanje u smernice: ESC/EAS
2023–2026 uključuje inclisiran u standardni algoritam za vrlo visok
rizik a ADA ga preporučuje ako terapijska adherencija predstavlja
problem [5–7].
Fibrati
Fenofibrat i Bezafibrat. Indikacije za fibrate: trigliceridi >5,6
mmol/L (>500 mg/dL), prevencija pankreatitisa, rezidualna
hipertrigliceridemija kod DM2.
Omega 3 masne kiseline (EPA formulacije) - visoke doze EPA (2–4 g/d)
koriste se za smanjenje TG i stabilizaciju plaka. REDUCE IT studija
pokazala je smanjenje KV ishoda kod pacijenata sa povišenim TG [39].
NOVINE U SMERNICAMA 2023–2026 (ADA, ESC/EAS, AHA/ACC)
U poslednje tri godine došlo je do nekoliko važnih promena koje
značajno utiču na svakodnevnu kliničku praksu. (Tabela 3 i Shema 2.)
Shema 2. Grafički prikaz terapiskog algoritma i
poređenja smernica
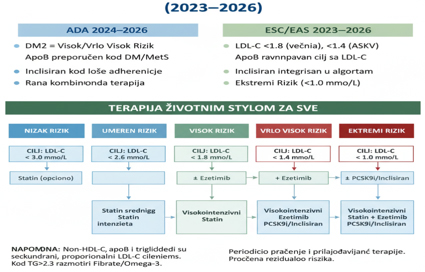
Tabela 3. Uporedni LDL C ciljevi po smernicama (ADA, AHA/ACC,
ESC/EAS)
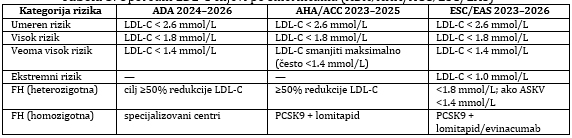
1. ADA 2024–2026 – Dijabetes i dislipidemija
Pacijenti sa DM2 automatski spadaju u kategoriju visokog ili veoma
visokog rizika. LDL C cilj kod većine dijabetičara: <1,8 mmol/L, a
kod ASKV<1,4 mmol/L. Preporučeno je merenje apoB kod osoba sa
gojaznošću, metaboličkim sindromom i visokim TG a inklisiran je
preporučen kod loše adherencije. Naglasak je na ranoj primeni
kombinovane terapije.
2. AHA/ACC 2023–2025 - personalizovani pristup terapiji; PCSK9
inhibitori sve češće već nakon prvog infarkta; LDL C cilj: “što
niže, to bolje”, ali bez formalnog numeričkog cilja u nekim
situacijama; važnost doživotnog praćenja LDL C kod pacijenata sa FH;
snažna uloga ne HDL C kod pacijenata sa visokom koncentracijom TG.
3. ESC/EAS 2023–2026 – Najagresivniji pristup LDL C. Uvedena je
kategorija “ekstremni rizik” polivaskularna bolest, ponovljeni ACS).
LDL C ciljevi: visok rizik <1,8 mmol/L, veoma visok rizik <1,4
mmol/L, ekstremni rizik <1,0 mmol/L. LDL C, non HDL C i apoB su
ravnopravni ciljni parametri; inclisiran zvanično uključen u
terapijski algoritam; snažniji naglasak na redukciji remnantnih
lipoproteina i TG.
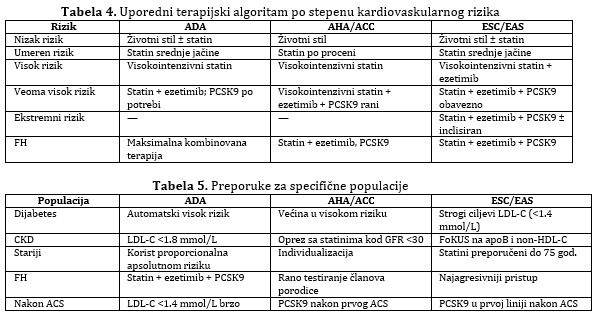
Terapijski uporedni algoritam po stepenu kardiovaskularnog rizika je
prikazan na Tabeli 4 i 5.
1. Efekat snižavanja LDL holesterola na kardiovaskularne ishode
U velikoj metaanalizi Cholesterol Treatment Trialists'
Collaboration, koja je obuhvatila više od 170.000 pacijenata,
pokazano je da svako smanjenje LDL C za 1 mmol/L (~39 mg/dL)
redukuje rizik od velikih vaskularnih događaja za oko 22% [23]. Ovaj
efekat je prisutan kod muškaraca i žena, kod mlađih i starijih, kod
dijabetičara, kod pacijenata sa prethodnim infarktom miokarda i u
primarnoj i sekundarnoj prevenciji. Snižavanje LDL C je korisno u
gotovo svim kliničkim populacijama.
2. Statini – dokazi iz kliničkih studija
Visokointenzivni statini dokazano smanjuju infarkt miokarda za
25–35%, ishemijski moždani udar za 20–30%, kardiovaskularnu smrt za
15–20% [6–8]. Pored LDL redukcije, statini imaju i pleiotropne
efekte stabilizaciju plaka, antiinflamatorno dejstvo i poboljšanje
endotelne funkcije [24].
3. Ezetimib – klinički ishodi
IMPROVE IT studija (ezetimib + statin) pokazala je dodatno
snižavanje LDL C za ~23%, 6% relativno smanjenje primarnog KV ishoda
(p=0.016) [11]. Ovo potvrđuje važnost kombinovane terapije.
4. PCSK9 inhibitori – najveći benefit kod najrizičnijih pacijenata
FOURIER studija (evolokumab) pokazuje LDL C smanjen na ~0,8 mmol/L,
15% redukcija KV događaja, 27% smanjenje rizika od infarkta miokarda
[10]. ODYSSEY Outcomes (alirokumab) značajno smanjenje KV
mortaliteta nakon akutnog koronarnog sindroma [11]. Ključnoje: što
je LDL C niži – korist je veća.
5. Inclisiran – nova era dugotrajne kontrole lipida
Inclisiran, kao siRNA terapija, smanjuje LDL C trajno i stabilno.
Prednosti su primena na svakih 6 meseci, bolja adherencija i ~50%
redukcije LDL C [12]. Još uvek se očekuju velike studije ishoda, ali
dosadašnji podaci su obećavajući.
6. Trigliceridi i rezidualni rizik
Povišeni trigliceridi i remnantske čestice lipoproteina značajno
povećavaju rizik od KV događaja, naročito kod pacijenata sa
dijabetesom i metaboličkim sindromom [19–20]. REDUCE IT studija (EPA
4 g/dan) pokazala je 25% redukciju velikih KV događaja i 20%
smanjenje KV mortaliteta [39]. Ovo potvrđuje da je rezidualni rizik
važan i da nije dovoljan samo LDL C.
NAJNOVIJE AMERIČKE PREPORUKE ZA LEČENJE DISLIPIDEMIJA IZ 2026
Nove američke preporuke preporuke [40] vraćaju fokus na ciljne
vrednosti LDL holesterola: kod pacijenata sa graničnim ili
intermedijarnim rizikom ciljne vrednosti su <2,6 mmol/L, kod
visokorizičnih pacijenata <1,8 mmol/L, a kod pacijenata sa veoma
visokim rizikom (tj. u sekundarnoj prevenciji) treba težiti
vrednostima LDL <1,4 mmol/L.
Usvojen je PREVENT-ASCVD kalkulator, koji predviđa 10-godišnji i
30-godišnji rizik od neželjenih kardiovaskularnihdogađaja (infarkt
miokarda, moždani udar ili kardiovaskularni mortalitet).
Karakteristike pacijenata koje su važne za procenu ovog rizika su
starost, pol, sistolni krvni pritisak, antihipertenzivna terapija,
prisustvo dijabetesa, status pušenja, kao i laboratorijski markeri
(ukupan i LDL holesterol). Ovo su neophodne varijable za osnovni
model. Kod proširenog modela potreban je podatak o indeksu telesne
mase (BMI) i bubrežnoj funkciji, dok potpuni model uključuje i
albuminuriju i HbA1c [40].
Novost je procena osim 10-godišnji kardiovaskularni rizik i
30-godišnji rizik za osobe starosti između 30 i 59 godina. Nove
preporuke osnažuju primenu dodatnih biomarkera za procenu
rezidualnog kardiovaskularnog rizika, kao što je lipoprotein(a),
čije se određivanje savetuje jednom u životu, kao i apolipoprotein
B, koji je posebno koristan kod pacijenata sa dijabetesom i
hipertrigliceridemijom.
Veća pažnja se pridaje određivanju koronarnog kalcijumskog skora
(CAC) [40], naročito u slučajevima neizvesnosti da li započeti
terapiju statinima ili ne. To je najčešće slučaj kod pacijenata sa
graničnim ili intermedijarnim rizikom. Važan deo novih preporuka
odnosi se na ranije i intenzivnije smanjenje LDL holesterola. Ovo se
oslanja na koncept da duže izlaganje povišenom LDL holesterolu
određuje kardiovaskularni rizik. Stoga je važno ranije uvesti
terapiju i tako smanjiti izlaganje visokom LDL holesterolu, što
dovodi do izraženije redukcije kardiovaskularnog rizika. S tim u
vezi, komplementarna preporuka jeste univerzalni lipidni skrining i
prevencija tokom života. Ne treba čekati na razvoj kardiovaskularnih
događaja, već se savetuje periodična provera lipidnog statusa, uz
poseban osvrt na skrining osoba sa dijabetesom,
kardio-renalno-metaboličkim sindromom kao i kod dece [40].
PROGNOZA
Dislipidemije, ako se ne dijagnostikuju i ne leče adekvatno,
značajno povećavaju rizik od aterosklerotske kardiovaskularne
bolesti, prerane invalidnosti i smrtnosti. Međutim, savremeni
terapijski pristupi omogućavaju dramatično poboljšanje prognoze.
1. Prognoza
Prognoza zavisi od početnih vrednosti LDL C, prisustva
komorbiditeta, stepena adherencije, genetskih faktora (posebno kod
FH) i pravovremenosti terapije. Kod pacijenata koji postižu ciljne
vrednosti LDL C prema ESC/EAS (<1.4 mmol/L za visok rizik), rizik od
novih KV događaja može se smanjiti i do 50% [5].
2. Kliničke implikacije
Savremene smernice 2023–2026 podvlače sledeće principe: LDL C je
glavni terapeutski cilj, Niži LDL C = bolja prognoza. Kombinovana
terapija je pravilo, a ne izuzetak. Statin + ezetimib + PCSK9
inhibitor / inclisiran. ApoB i non HDL C su jednako važni kao i LDL
C. Posebno kod pacijenata sa visokim trigliceridima i dijabetesom.
Personalizacija terapije. Različiti ciljevi za različite kategorije
rizika.
KARDIOVASKULARNI BENEFITI I ISHODI
Snižavanje aterogenih lipoproteina, posebno LDL holesterola,
predstavlja najefikasniju farmakološku strategiju u prevenciji
aterosklerotske kardiovaskularne bolesti (ASKV). Brojne
randomizovane kliničke studije, genetičke analize i meta analize
pokazuju jasnu uzročnu vezu između redukcije LDL C i smanjenja
rizika od velikih kardiovaskularnih događaja [8–12,25–34].
1. Efekat snižavanja LDL holesterola na kardiovaskularne ishode
U velikoj metaanalizi Cholesterol Treatment Trialists'
Collaboration, koja je obuhvatila više od 170.000 pacijenata,
pokazano je da svako smanjenje LDL C za 1 mmol/L (~39 mg/dL)
redukuje rizik od velikih vaskularnih događaja za oko 22% [25]. Ovaj
efekat je prisutan kod muškaraca i žena, kod mlađih i starijih, kod
dijabetičara, kod pacijenata sa prethodnim infarktom miokarda i u
primarnoj i sekundarnoj prevenciji. Snižavanje LDL C je korisno u
gotovo svim kliničkim populacijama.
2. Statini – dokazi iz kliničkih studija
Visokointenzivni statini dokazano smanjuju infarkt miokarda za
25–35%, ishemijski moždani udar za 20–30%, kardiovaskularnu smrt za
15–20% [8–10]. Pored LDL redukcije, statini imaju i pleiotropne
efekte stabilizaciju plaka, antiinflamatorno dejstvo i poboljšanje
endotelne funkcije [26].
3. Ezetimib – klinički ishodi
IMPROVE IT studija (ezetimib + statin) pokazala je dodatno
snižavanje LDL C za ~23%, 6% relativno smanjenje primarnog KV ishoda
(p=0,016) [11]. Ovo potvrđuje važnost kombinovane terapije.
4. PCSK9 inhibitori – najveći benefit kod najrizičnijih pacijenata
FOURIER studija (evolokumab) pokazuje LDL C smanjen na ~0,8 mmol/L,
15% redukcija KV događaja, 27% smanjenje rizika od infarkta miokarda
[8]. ODYSSEY Outcomes (alirokumab) značajno smanjenje KV mortaliteta
nakon akutnog koronarnog sindroma [9]. Ključno je: što je LDL C niži
– korist je veća.
5. Inclisiran – nova era dugotrajne kontrole lipida
Inclisiran, kao siRNA terapija, smanjuje LDL C trajno i stabilno.
Prednosti su primena na svakih 6 meseci, bolja adherencija i ~50%
redukcije LDL C [12]. Još uvek se očekuju velike studije ishoda, ali
dosadašnji podaci su obećavajući.
6. Trigliceridi i rezidualni rizik
Povišeni trigliceridi i remnantske čestice lipoproteina značajno
povećavaju rizik od KV događaja, naročito kod pacijenata sa
dijabetesom i metaboličkim sindromom [19–20]. REDUCE IT studija (EPA
4 g/dan) pokazala je 25% redukciju velikih KV događaja i 20%
smanjenje KV mortaliteta [39]. Ovo potvrđuje da je rezidualni rizik
važan i da nije dovoljan samo LDL C.
GENSKA TERAPIJA I BUDUĆE PERSPEKTIVE [41]
In vivo gensko ili bazno uređivanje (GENE OR BASE EDITING)
predstavlja novu terapijsku strategiju koja se u poslednje vreme
testira za lečenje dislipidemija ciljajući gene PCSK9 i ANGPTL3.
VERVE-101 je eksperimentalna terapija zasnovana na CRISPR baznom
uređivanju, koja sadrži mRNA za adeninski bazni editor usmeren na
gen PCSK9, sa ciljem trajnog „utišavanja“ (inaktivacije) tog gena
[42].
Kod ne-ljudskih primata, infuzija leka VERVE-101 dovela je do
smanjenja LDL-C za 69% uz postojan efekat do 476 dana nakon
doziranja, bez značajnih neželjenih događaja. Nakon potvrđene
efikasnosti kod primata, prva studija na ljudima obuhvatila je 10
pacijenata sa heterozigotnom porodičnom hiperlipidemijom (HeFH) i
prosečnim nivoom LDL-C od 201 mg/dL. Jedna intravenozna infuzija
genske terapije zasnovane na CRISPR tehnologiji putem ciljano
usmerenih lipidnih nanočestica dovela je do značajnog smanjenja
LDL-C do 55% [43]. Naslednik pomenute terapije, Verve-102,
predstavlja sredstvo za bazno uređivanje gena PCSK9 sa unapređenim
usmeravanjem na jetru i redizajniranim nanočesticama, i trenutno je
u fazi kliničkog razvoja. Danas raspolažemo brojnim efikasnim
strategijama za suzbijanje lipidnih faktora rizika za
kardiovaskularne bolesti (KVB). Još obećavajuće inovacije
nagoveštavaju dalji napredak u ovoj oblasti. Međutim, primena
dokazanih terapija, prihvatanje od strane pacijenata, doslednost u
sprovođenju lečenja i obezbeđivanje pravednog pristupa savremenim
terapijskim dostignućima ostaju izazovi koje zajednica mora da
prevaziđe [4].
ZAKLJUČAK
Dislipidemije ostaju jedan od najvažnijih faktora rizika za
aterosklerozu i kardiovaskularni mortalitet. Snižavanje aterogenih
lipoproteina, posebno LDL holesterola, predstavlja najefikasniju
farmakološku strategiju u prevenciji aterosklerotske
kardiovaskularne bolesti (ASKV). Brojne randomizovane kliničke
studije, genetičke analize i meta analize pokazuju jasnu uzročnu
vezu između redukcije LDL C i smanjenja rizika od velikih
kardiovaskularnih događaja Napredak u razumevanju lipidnog
metabolizma i dostupnost novih terapija značajno su unapredili
mogućnosti lečenja. Integracija preporuka ADA, AHA/ACC i ESC/EAS
omogućava optimalan i individualizovan pristup, posebno kod
bolesnika sa visokim i veoma visokim rizikom. Novost američkog
vodiča ACC/AHA iz 2026. godine je procena osim 10-godišnjeg
kardiovaskularnog nefatalnog i fatalnog rizika i rizik i 30-godišnji
rizik za osobe starosti između 30 i 59 godina. Nove preporuke
osnažuju primenu dodatnih biomarkera za procenu rezidualnog
kardiovaskularnog rizika, kao što je lipoprotein(a), apolipoprotein
B, ne-HDL holesterol, koronarni kalcijumski skor , indeks telesne
mase i A1C kao i apolipoprotein B, koji je posebno koristan kod
pacijenata sa dijabetesom i hipertrigliceridemijom.Nastavak
istraživanja u oblasti lipidologije, razvoj novih lekova i
unapređena genetska dijagnostika doprineće još efikasnijoj
prevenciji ASKV u budućnosti.
REFERENCE :
1. European Society of Cardiology. ESC Guidelines for the
Management of Myocarditis and Pericarditis. Eur Heart J. 2025.
2. European Society of Cardiology. 2015 ESC Guidelines on
Pericardial Diseases. Eur Heart J. 2015;36:2921–2964.
3. American College of Cardiology. ACC Expert Consensus Decision
Pathway on Myocarditis. J Am Coll Cardiol. 2024.
4. American College of Cardiology. ACC Consensus on Pericardial
Diseases. J Am Coll Cardiol. 2024.
5. Caforio ALP, Pankuweit S, Arbustini E, et al. Current state of
knowledge on aetiology, diagnosis and therapy of myocarditis. Eur
Heart J. 2022;43:399–421.
6. Ammirati E, Frigerio M, Adler ED, et al. Management of acute
myocarditis and chronic inflammatory cardiomyopathy. Circulation.
2022;145:1722–1737.
7. Cooper LT. Myocarditis. N Engl J Med. 2009;360:1526–1538.
8. Tschöpe C, Ammirati E, Bozkurt B, et al. Myocarditis and
inflammatory cardiomyopathy: current evidence and future directions.
Nat Rev Cardiol. 2021;18:169–193.
9. Kindermann I, Barth C, Mahfoud F, et al. Update on myocarditis. J
Am Coll Cardiol. 2022;79:1326–1342.
10. Friedrich MG, Sechtem U, Schulz Menger J, et al. Cardiovascular
magnetic resonance in myocarditis: a JACC White Paper. J Am Coll
Cardiol. 2009;53:1475–1487.
11. Ferreira VM, Schulz Menger J, Holmvang G, et al. CMR mapping
techniques for myocarditis: consensus statement. JACC Cardiovasc
Imaging. 2018;11:155 169.
12. Bastać D, Marković Z, Vasić B, et al. Dijastolni stres test u
proceni bolesnika sa srčanom insuficijencijom. Zbornik radova
Zdravstvenog centra Zaječar. 2017;1:45–49.
13. Bastać D, Vasić B, Nešović P, et al. Ehokardiografska procena
dijastolne funkcije kod bolesnika sa miokarditisom. Timočki
medicinski glasnik. 2018;43(2):73–78.
14. Bastać D, Vasić B, Marković Z, et al. Srčana insuficijencija sa
očuvanom ejekcionom frakcijom – dijagnostički izazovi. Timočki
medicinski glasnik. 2020;45(1):23–28.
15. Heymans S, Cooper LT, De Smet B, et al. Inflammatory
cardiomyopathy. Eur Heart J. 2020;41:1358–1376.
16. Schultheiss HP, Kühl U, Cooper LT. Viral myocarditis. Nat Rev
Cardiol. 2021;18:145–161.
17. Imazio M, Klingel K, Kindermann I, et al. Myocarditis
management – current trends and future perspectives. Eur Heart J.
2022;43:1012–1027.
18. Kühl U, Pauschinger M, Noutsias M, et al. Viral persistence in
myocardium is associated with progressive cardiac dysfunction.
Circulation. 2005;112:1965–1970.
19. Ammirati E, Veronese G, Bottiroli M, et al. Contemporary
management of myocarditis: diagnostic and therapeutic updates. Eur J
Heart Fail. 2024;26:1–15.
20. Ammirati E, Cipriani M, Lilliu M, et al. Clinical presentation
and outcome of myocarditis. Eur J Heart Fail. 2020;22:2117–2125.
21. McCarthy RE III, Boehmer JP, Hruban RH, et al. Long term outcome
of fulminant myocarditis as compared with acute (nonfulminant)
myocarditis. N Engl J Med. 2000;342:690–695.
22. Blauwet LA, Cooper LT. Myocarditis. Prog Cardiovasc Dis.
2010;52:274–288.
23. Frustaci A, Russo MA, Chimenti C. Randomized study on the
efficacy of immunosuppressive therapy in virus negative inflammatory
cardiomyopathy. N Engl J Med. 2009;360:1526–1538.
24. Cooper LT, Berry GJ, Shabetai R. Giant cell myocarditis. N Engl
J Med. 1997;336:1860–1866.
25. Siripanthong B, Nazarian S, Muser D, et al. Recognizing COVID
19–related myocarditis: the possible pathophysiology and proposed
diagnostic algorithm. Heart Rhythm. 2020;17:1463–1471.
26. Puntmann VO, Carerj L, Wieters I, et al. Outcomes of
cardiovascular magnetic resonance imaging in patients recently
recovered from COVID 19. JAMA Cardiol. 2020;5:1265–1273.
27. Mevorach D, Anis E, Cedar N, et al. Myocarditis after
BNT162b2 mRNA COVID 19 vaccination. N Engl J Med.
2021;385:2140–2149.
28. Witberg G, Barda N, Hoss S, et al. Myocarditis after COVID 19
vaccination in patients under 40 years. N Engl J Med.
2021;385:1813–1822.
29. Bozkurt B, Kamat I, Hotez PJ. Myocarditis with COVID 19 mRNA
vaccines. Circulation. 2021;144:471–484.
30. Oster ME, Shay DK, Su JR, et al. Myocarditis cases reported
after mRNA based COVID 19 vaccination in the US. JAMA.
2022;327:331–340.
|
|
|
|





